Современный подход к терапии массивных акушерских кровотечений

Фото носит иллюстративный характер. Из открытых источников.
На 3-м Минском медицинском международном форуме доцент кафедры детской анестезиологии и реаниматологии ИПКиПКЗ БГМУ, кандидат мед. наук, главный внештатный анестезиолог-реаниматолог по акушерско-гинекологической помощи комитета по здравоохранению Мингорисполкома, врач-анестезиолог-реаниматолог городского клинического родильного дома № 2 Минска Алексей Жаворонок выступил с докладом, посвященным современным подходам в терапии массивных акушерских кровотечений.
Проблемные моменты
Массивные акушерские кровотечения занимают первое место в структуре причин материнской смертности во всем мире. Поздние роды и увеличение экстрагенитальной патологии у матери, а также числа кесаревых сечений требуют создания индивидуального мультидисциплинарного подхода к каждой пациентке. Согласно данным за 2023 год, опубликованным в европейском журнале «Анестезиология», причиной 60 % всех акушерских кровотечений является тонус — нарушение сократительной способности матки (гипо- или атония), 20 % — травма половых органов, разрыв матки, 10 % — задержка плацентарной ткани. На тромбин, нарушение коагуляции приходится всего 1,9 %. Этиология акушерских кровотечений настолько многообразна, что нужно понимать и знать все эти составляющие.
Лечение массивных кровотечений должно осуществляться одновременно в нескольких направлениях. Это оценка объема кровопотери, применение утеротоников, антифибринолитиков (транексамовой кислоты), баллонная тампонада и/или хирургическая остановка кровотечения, нормализация гемодинамики (поддержание сердечного выброса), поддержание pH, температуры, ионизированного кальция, кислородной емкости крови и коррекция системы гемостаза.

— Самым сложным в терапии массивного кровотечения являются два направления. Это оценка объема кровопотери и первоначальная инфузионная терапия, потому что недооценка объема кровопотери ведет к неверно выбранной тактике инфузионно-трансфузионной терапии, которая может привести к увеличению объема кровопотери и, соответственно, утяжелению состояния пациента. С другой стороны, переоценка объема кровопотери в свою очередь может привести к тромбозам и/или трансфузионно-ассоциированной циркуляционной перегрузке легких, — говорит Алексей Жаворонок.
Нормализация гемодинамики — сложнейший момент оказания помощи пациенту с массивным кровотечением. На начальном этапе рекомендуется использовать стратегию с целевым систолическим артериальным давлением 80–90 мм рт. ст. (среднее АД 50–60 мм рт. ст.) до тех пор, пока не будет остановлено кровотечение.
Ставка на совокупность методов
— В чем же сложности этапа оценки объема кровопотери? Есть несколько методов оценки, согласно современным международным рекомендациям. Но нет ни одного метода, который бы 100 % вам сказал, какое количество крови потерял пациент, — объясняет Алексей Жаворонок.
К сожалению, наиболее частый метод оценки кровопотери — это визуальный. А его ошибка достигает 30–50 %.
По словам специалиста, из-за неадекватной оценки массивности кровопотери зачастую применяется неправильно выбранная тактика, которая в результате сопровождается увеличением объема кровопотери и утяжелением состояния пациента.
— Еще один из методов оценки объема кровопотери — гравиметрический, ошибка которого составляет 15 %. Он рекомендуется сегодня многими авторитетными источниками. Однако и в данном случае есть вопрос по его применению именно к акушерским кровотечениям. Околоплодные воды изливаются и смешиваются с кровью. И если все это взвесить, ошибка будет гораздо выше, чем обещанные 15 %. При измерении мерной емкостью (лоток, кружка с мерной градуировкой) ошибка достигает 20 %, — перечисляет специалист. — Кроме того, в последнее время в международных рекомендациях снова появилась незаслуженно забытая методика, которой нас учили еще в мединституте, — шоковый индекс Альговера. Его можно успешно использовать как динамический показатель эффективности проводимой терапии. И кстати, независимо от видимой кровопотери при наличии клинических признаков геморрагического шока (шоковый индекс более 0,9) следует предполагать послеродовое кровотечение.
Еще один весьма проблемный момент — оценка объема кровопотери по гемоглобину. Начинается кровотечение, оно прогрессирует, снижается АД и увеличивается частота сердечных сокращений (ЧСС). Доктор инициирует выполнение общего анализа крови, назначает инфузионную терапию, цель которой повысить АД и снизить ЧСС. Позже повторяется общий анализ крови, и часто результат пугает.
К примеру, изначально гемоглобин 100, а потом на фоне массивной инфузионной терапии берется еще один анализ. В этот раз гемоглобин падает уже до 60. Все удивляются: «У нас же не было такой большой кровопотери за это время, как так?»
Проблема в том, что пациент теряет цельную кровь, уменьшается объем циркулирующей крови, увеличивается шоковый индекс Альговера, и на этом этапе гемоглобин в общем анализе крови будет еще в нормальных значениях. А вот после начала инфузионной терапии, цель которой снизить шоковый индекс Альговера, происходит разведение гемоглобина (дилюция).
Важно помнить:
Алексей Жаворонок напоминает, что невозможно сделать ставку на один метод. Поэтому оценивать кровопотерю нужно по совокупности нескольких методов.
Одно из новшеств, которое меня очень сильно порадовало и которое позволяет быстро оценить ситуацию, — это дефицит буферных оснований, критерий, указанный в европейских рекомендациях 2023 года по ведению кровотечений в травме.По личному опыту могу сказать: этот показатель действительно работает. При кровотечении инициируем выполнение КОС и смотрим BE, в зависимости от этого показателя видим класс кровотечения, с которым столкнулись.
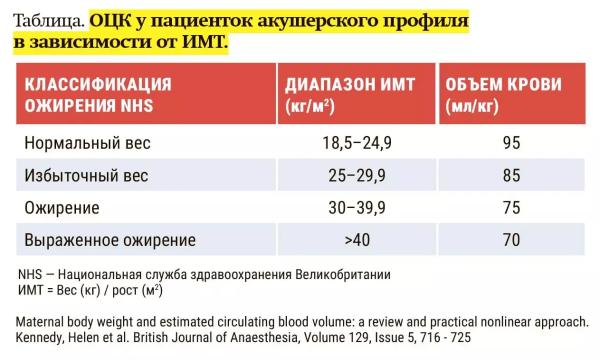
— Оценка объема кровопотери — очень важный момент, но вместе с тем это всего лишь 50 % поставленной задачи. Вторые 50 % — это необходимость правильно рассчитать ОЦК (объем циркулирующей крови) беременной женщины. И здесь тоже кроются свои сложности, в частности, в коэффициентах. К сожалению, оказалось: коэффициент 75 мл/кг, которому нас обучали, не совсем эффективный, поскольку он немного заниженный. В российских рекомендациях указан другой коэффициент — 100 мл/кг. Например, женщина весит 120 кг. Но если применить данный коэффициент, у нее ОЦК будет 12 литров. Но разве это может быть так? Нет, все прекрасно знают: увеличение жировой массы не коррелирует с увеличением объема циркулирующей крови, — рассуждает Алексей Жаворонок.
В 2022 году была опубликована одна из последних европейских рекомендаций по поводу оценки ОЦК у пациенток акушерского профиля по индексу массы тела (см. таблицу). Предлагается отказаться от применения линейных формул (массу тела умножить на коэффициент) и использовать коэффициент расчета ОЦК на основе индекса массы тела. В зависимости от увеличения ИМТ этот коэффициент снижается.
Контроль всех причин
В развитии коагулопатии выделяют следующие причины: разведение, ацидоз и снижение ионизированного кальция, гипотермия, гипоперфузия, гиперфибринолиз, потеря плазмы, факторов коагуляции и тромбоцитов. И в этом как раз таки и таится сложность коррекции системы гемостаза и вообще оказания помощи пациентам с кровотечением. Потому что обязательно нужно контролировать все эти причины.
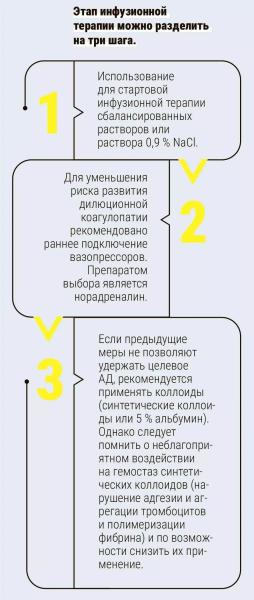
— Суть инфузионной терапии заключается в поддержании среднего АД до момента появления препаратов крови. В дальнейшем необходимо ограничивать инфузионную терапию, переходя к стратегии восполнения препаратами крови. Не надо проводить пациентам избыточную инфузионную терапию, потому что на этом этапе вы своими руками можете создать дилюционную коагулопатию. Необходим взвешенный подход, — подчеркивает Алексей Жаворонок.
Не нужно забывать о раннем применении (в течении первых 3-х часов) антифибринолитиков, где препаратом выбора является транексамовая кислота, которая рекомендована всеми международными сообществами.
Важными этапами оказания помощи пациенту с массивным кровотечением являются:
Один из первых препаратов крови, который должен быть в распоряжении, — эритроцитарная масса, необходимая для поддержания кислородной емкости крови. С ее применением связано несколько стратегий в коррекции гемостаза. Шаги складываются из диагностики, начальной гемостатической терапии и/или протокола массивной трансфузии и/или гемостатической реанимации. При этом ставка делается не на один метод, а на их совокупность.
Если рассматривать коагулопатию с точки зрения плазменного гемостаза, то в ее развитии можно выстроить определенную стадийность.
Ранним признаком коагулопатии является дефект плотности тромба, за счет резкого снижения фибриногена.
Например, если у пациента изначально фибриноген по Клаусу был равен 4 г/л и потом стал 2 г/л, а кровотечение продолжается, то ждать, когда он будет ниже критического уровня (1,5 г/л по Клаусу), не надо. Поэтому на этом этапе, если продолжается кровотечение и фибриноген <2 г/л по Клаусу, его необходимо сразу же корригировать и поддерживать целевой уровень выше 2 г/л. Трансфузия 3 г фибриногена ожидаемо повысит уровень фибриногена по Клаусу в коагулограмме на 1 г/л либо на 6 мм в тесте FIBTEM A5 по данным тромбоэластометрии. Резкое снижение фибриногена является ранним признаком коагулопатии и маркером прогрессирования кровотечения, поэтому раннее выявление его снижения имеет решающее значение. Дальше можно выстроить следующую закономерность.
Запускается механизм нарушения стабильности тромба — фибринолиз, поэтому наряду с инфузионной терапией в случае кровотечения назначают транексамовую кислоту.
На следующем этапе возникает дефицит факторов свертывания — длительное образование тромба. И самый поздний признак — это дефицит XIII фактора.
— Для диагностики системы гемостаза у нас существуют два варианта: коагулограмма и методы, основанные на изучении вязкоэластических свойств сгустка, — тромбоэластометрия (ROTEM)/тромбо-эластография (TEG). Все перинатальные центры и гинекологическая больница Минска оборудованы тромбоэластометрами, — поясняет Алексей Жаворонок.
Хочется акцентировать внимание: применение TEG/ROTEM сократило время диагностики коагулопатии и, соответственно, повысило скорость реакции врача на динамически изменяющуюся ситуацию в системе гемостаза и дало возможность своевременно корригировать его под контролем TEG/ROTEM.
— К примеру, данные коагулограммы мы получаем через 45–60 минут. Учитывая массивность акушерских кровотечений, когда за 30–40 минут можно потерять ОЦК, мы не будем ждать результатов данного анализа, и инфузионно-трансфузионная стратегия будет строиться эмпирически. В то же время при применении TEG/ROTEM время от забора материала до получения релевантных результатов, на которых мы строим свою терапию, составляет 7–10 минут, — комментирует специалист. — Кроме того, диагностическая ценность TEG/ROTEM заключается в том, что данное оборудование позволяет выявить конкретные причины нарушения гемостаза, применить целенаправленную терапию вместо мультитрансфузионного подхода. А целенаправленная коррекция снижает расход компонентов крови (включая эритроцитарную массу), повышая безопасность и эффективность терапии, экономию средств. Основное преимущество диагностики TEG/ROTEM заключается в том, что данные методы помогают отличить хирургическое кровотечение от коагулопатического и, соответственно, позволяют снизить необоснованное назначение свежезамороженной плазмы (СЗП).
Если кровотечение продолжается, а в результатах TEG/ROTEM все показатели в норме, то причина кровотечения не коагулопатия и переливать СЗП не нужно, необходимо наладить хирургический гемостаз. Показание для переливания СЗП лишь одно — восполнение дефицита факторов свертывания.
Актуальные стратегии
В зависимости от класса кровотечения (их четыре, и градация основана на проценте потери ОЦК) можно выделить несколько стратегий терапии массивных акушерских кровотечений.
Согласно европейским рекомендациям 2023 года, есть два основных подхода к терапии массивных кровотечений для начального восстановления коагуляции.
Один из них более известный — применение эритроцитарной массы в совокупности с СЗП/вирусинактивированной плазмой в соотношении препаратов крови 2:1 либо в соотношении 1:1 (1С).
Вторая стратегия — использование эритроцитарной массы и коррекция плазменного гемостаза с помощью либо криопреципитата, либо концентрата фибриногена. И в дальнейшем возможно переходить к мультитрансфузионному подходу (комбинированное применение свежезамороженной плазмы с добавлением фибриногена и/или концентратов протромбинового комплекса) либо к селективной терапии концентратами факторов свертывания крови.
В первом случае рекомендуется избегать трансфузий СЗП вне массивного кровотечения. При использовании стратегии на основе СЗП необходимо провести мониторинг параметров коагуляции и при необходимости дополнить терапию еще и концентратами факторов (1С). Согласно международным рекомендациям 2023 года, необходимо как можно раньше переходить к целенаправленной терапии.
Отдельно можно выделить стратегию при четвертом классе кровотечения — потеря ОЦК >40 % (> 2 400 мл у пациента акушерского профиля с ИМТ 26 — коэффициент (объем крови) 85 мл/кг, масса тела 70 кг. Расчет ОЦК = 70×85 =5 950 мл).
В данном случае требуется применение протокола массивной трансфузии, который включает, на фоне введения 15–20 мг/кг транексамовой кислоты, трансфузию 4 гемаконов эритроцитарной массы и 4 гемаконов СЗП, при наличии TEG/ROTEM как можно скорее рекомендуется перейти к целенаправленной терапии. В случае отсутствия TEG/ROTEM к 4 гемаконам эритроцитарной массы и 4 гемаконам СЗП эмпирически добавляется 3–4 г фибриногена либо по содержанию в криопреципитате (1 доза криопреципитата приблизительно содержит 140 мг фибриногена), либо 3–4 г концентрата фибриногена, при необходимости в протокол массивной трансфузии добавляется тромбоцитарная масса.
Протокол массивной трансфузии должен быть разработан и утвержден в каждом стационаре в соответствии с диагностическими возможностями, обеспечением лекарственными средствами и логистическими особенностями.
Пример целенаправленного протокола массивной трансфузии представлен в приложении 16 постановления Министерства здравоохранения от 1 апреля 2022 г. № 24 (клинический протокол «Оказание медицинской помощи женщинам с послеродовыми кровотечениями в стационарных условиях»).
Основные проблемы управления рисками послеродовых кровотечений — это запоздалая диагностика и/или лечение, недооценка объема кровопотери, а также задержка или отсутствие обеспечения препаратами крови.
Негативно сказываются на эффективности и безопасности оказываемой помощи недостаточный уровень знаний, отсутствие обучения, слабая коммуникация в рамках междисциплинарной команды, отсутствие протоколов или их нарушение, недочеты либо пробелы в организационной структуре.
— Благодаря специалистам Минздрава и комитета по здравоохранению Мингорисполкома делается все максимально для того, чтобы повысить эффективность и безопасность оказываемой помощи пациентам с массивной кровопотерей как в Минске, так и в стране. Учреждения родовспоможения столицы оснащены всеми препаратами и инфузионно-трансфузионными средами для оказания помощи пациентам при массивном кровотечении, проводятся регулярные тренинги, обучающие семинары и конференции, дооснащение необходимым оборудованием для прикроватной диагностики и высокоскоростной инфузии/трансфузии подогретых сред. Это позволяет оперативно реагировать на изменения в системе гемостаза и максимально быстро проводить целенаправленную терапию. Суть данной стратегии можно выразить словами: «Не анализы пациента отправлять в лабораторию, а лаборатория должна быть возле пациента». Такой подход позволяет снизить объемы кровопотери за счет быстрой реакции на динамически меняющуюся ситуацию в системе гемостаза, с пониманием врачом проводимой им терапии, — говорит Алексей Жаворонок.
Отделения анестезиологии и реанимации получают аппараты КОС по республиканской закупке. Применение прикроватного теста КОС в разрезе массивных кровотечений является важным компонентом оказания помощи: делается очень быстро (сроки, в которые выполняется анализ КОС, не должны превышать 5–10 минут), включает оксиметрию, определение рН, газов крови, электролитов (ионизированный кальций и т. д.) и метаболитов (лактат и BE), дает информацию о гематокрите и количестве гемоглобина. Это позволяет быстро корригировать систему гемостаза в условиях операционных или у постели пациента вместе с TEG/ROTEM, которые дают информацию о формировании сгустка (время, плотность и стабильность). Комитетом по здравоохранению Мингорисполкома планируется к закупке оборудование для высокоскоростной инфузионной терапии с подогревом растворов (аппараты типа Level 1).
Что касается альтернативы (замены) компонентов крови: для эритроцитов возможна только реинфузия, отмечает специалист. Для этого все перинатальные центры столицы оснащены аппаратами для реинфузии крови типа Cell Saver. Донаторы фибриногена — это криопреципитат либо концентрат фибриногена. Для факторов свертывания — СЗП, вирусинактивированная плазма, концентрат факторов протромбинового комплекса, фактор VII. Тромбоцитам альтернативы нет.
Для оказания эффективной помощи пациентам с массивными кровотечениями необходим запас препаратов крови для проведения протокола массивной трансфузии.
Для экстренной коррекции гипофибриногенемии необходимо иметь возобновляемый запас 3–4 г по фибриногену (3 г фибриногена повышают уровень фибриногена по Клаусу на 1 г/л в коагулограмме) и/или криопреципитат лиофилизат (рекомендуется криопреципитат лиофилизированный, так как он не требует разморозки в отличие от свежезамороженного).
В одной банке криопреципитата лиофилизата содержится 2 дозы — приблизительно 280 мг фибриногена, соответственно, минимально необходимое количество возобновляемого хранения препаратов — донаторов фибриногена, позволяющее выиграть время для возобновления запаса, должно составлять 11–14 банок криопреципитата лиофилизата каждой группы или 3–4 г концентрата фибриногена.
— То есть если вы получаете фибриноген в коагулограмме 1,5 г/л по Клаусу, вам необходимо дать 3–4 г фибриногена, чтобы выйти в итоге на показатель целевого уровня фибриногена >2 г/л по Клаусу. В данном случае мы ожидаем получить 2,5 г/л по Клаусу, но если кровотечение продолжается, то можно ожидать и более низкого значения фибриногена, несмотря на трансфузию 3–4 г фибриногена, — поясняет Алексей Жаворонок. — Вирусинактивированная плазма имеет стратегическое значение в протоколе массивной трансфузии, когда мы говорим об одномоментных массивных кровопотерях (>40 % ОЦК). Особенность вирусинактивированной плазмы в том, что она не имеет резус-принадлежности, а только групповую. Например, пациент поступает в операционную, минуя приемный покой. В операционной определяется группа крови и для выяснения резуса отправляется анализ в лабораторию. Мы запускаем протокол массивной трансфузии, который состоит из 4 гемаконов эритроцитарной массы и 4 гемаконов СЗП (которые еще нужно разморозить). Теряется время на определения резус-фактора. Поскольку есть групповая принадлежность, мы можем начинать протокол массивной трансфузии с размораживания и трансфузии вирус-инактивированной плазмы до появления данных о резус-факторе.
Таким образом, работа мультидисциплинарной команды с участием акушеров-гинекологов, анестезиологов, трансфузиологов, знание различных стратегий управления кровотечением позволяют сохранить жизнь и здоровье пациенток, обеспечив главный принцип родовспоможения — безопасность.
Источник: medvestnik.by